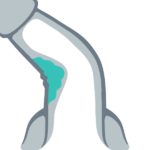
A doença de Peyronie (DP) é um distúrbio fibrótico da túnica albugínea peniana (TA) e pode causar dor durante a ereção e/ou relação sexual, curvatura peniana, disfunção erétil e deformidade e/ou encurtamento peniano, com consequências psicossociais e impacto nos pacientes e seus parceiros. Foi relatado que a DP afeta 0,3% a 13,1% dos homens na população em geral, e foi relatado que a prevalência aumenta com a idade, diabetes, hipertensão, hiperlipidemia, contratura de Dupuytren, tabagismo, consumo de álcool, prostatectomia pós-radical e disfunção erétil.
Embora a fisiopatologia exata da DP permaneça obscura, acredita-se que o trauma microvascular, ou trauma menor repetitivo, leva à inflamação na Túnica Albugínea (TA), o que desencadeia a liberação de citocinas pró-fibróticas, como o fator transformador de crescimento β1. Concentrações aumentadas do fator de crescimento transformador β1 por períodos prolongados devido à cicatrização de feridas não resolvidas levam, em última análise, à transformação de fibroblastos residentes em miofibroblastos profibróticos. Os miofibroblastos são responsáveis pela produção e deposição excessiva de proteínas da matriz extracelular, como o colágeno, que é então remodelado em uma placa fibrótica densa que pode causar o aparecimento de curvatura peniana e os sinais e sintomas relacionados à DP.
Pacientes com DP podem apresentar-se em 2 fases: aguda (instável) e crônica (estável). A fase aguda é caracterizada por inflamação na TA como resultado de trauma microvascular repetitivo, clínico ou subclínico. Nesta fase, a placa peniana começa a se formar e a elasticidade do TA é reduzida, resultando em curvatura. Normalmente, durante a fase aguda, os pacientes apresentam dor durante na ereção e/ou relação sexual, curvatura peniana e perda de comprimento. A duração da fase aguda é discutível: normalmente é de 4 a 6 meses e pode durar até 18 meses. Na fase crônica, que segue a fase aguda, a dor normalmente diminui e a placa torna-se mais organizada e estável e eventualmente pára de crescer.
Embora existam evidências clínicas limitadas para terapias que demonstrem eficácia consistente na fase aguda da DP, as opções para a DP crônica são limitadas à injeção de colagenase e à cirurgia. Infelizmente, a colagenase foi retirada do mercado do Reino Unido e da União Europeia e está atualmente disponível apenas no mercado dos EUA. A cirurgia tem sido tradicionalmente o padrão-ouro em pacientes com DP crônica, apesar dos riscos de encurtamento peniano, disfunção erétil ou dormência peniana, bem como recorrência da curvatura.
À medida que a conscientização sobre a DP aumentou no público em geral, mais homens apresentaram DP aguda na clínica nos últimos anos. As opções disponíveis que os médicos podem oferecer a esses pacientes são limitadas e nenhum deles foi licenciado para isso. Cada vez mais se destaca a necessidade significativa não atendida de desenvolvermos novas abordagens terapêuticas para DP aguda.
O reposicionamento de medicamentos demonstrou ser uma abordagem viável para doenças negligenciadas. Os miofibroblastos são as células-chave que impulsionam o processo fibrótico na DP aguda, e a prevenção da transformação de fibroblastos residentes em miofibroblastos profibróticos tem sido sugerida como uma abordagem terapêutica para retardar o progresso da fibrose. Como tal, já selecionamos um total de 1.954 medicamentos aprovados pela Food and Drug Administration, com a esperança de identificar aqueles que podem prevenir a transformação de miofibroblastos e depois serem reaproveitados para DP aguda. Usando esta abordagem de triagem, identificamos 26 medicamentos que podem prevenir a transformação de fibroblastos derivados de TA em miofibroblastos em pacientes com DP. Entre os medicamentos atingidos, duas classes foram observadas, pois foram sugeridas como potencialmente eficazes na DP aguda: inibidores da fosfodiesterase tipo 5 (PDE5is; por exemplo, sildenafil, vardenafil e tadalafil) e moduladores seletivos do receptor de estrogênio (SERMs ; por exemplo, tamoxifeno e raloxifeno).
Os SERMS atuam nos receptores estrogênicos do hipotálamo causando os níveis de FSH e LH.
Os PDE5is foram sugeridos pela primeira vez para o tratamento da DP aguda com base em evidências in vitro e in vivo. No entanto, os resultados dos estudos clínicos foram mistos. Foi sugerido que qualquer efeito observado dos PDE5is na curvatura pode ser devido à sua efeito pró-erétil, não necessariamente efeito antifibrótico, uma vez que o PDE5is pode causar ereções rígidas e, portanto, pode influenciar as medições da curvatura ou prevenir microtraumas adicionais.
Os estudos clínicos com tamoxifeno sugeriram um possível benefício clínico se o tratamento fosse iniciado dentro de 4 a 6 meses após os primeiros sinais ou sintomas. O tamoxifeno foi, no entanto, ineficaz em pacientes com DP crônica. Esses estudos clínicos iniciais sugerem que o momento do tratamento para apresentar algum benefício clínico é na fase aguda, retardando ou interrompendo a progressão da fibrose através da prevenção da formação de novos miofibroblastos. Isto é apoiado por pesquisas pré-clínicas de que estes medicamentos são capazes de prevenir a transformação de fibroblastos em miofibroblastos, mas não são capazes de reverter a transformação.
Esses estudos anteriores nos levaram a testar se uma combinação de PDE5i e SERM teria um efeito maior do que cada um de seus componentes. Utilizando técnicas de cultura celular in vitro e um modelo de DP de rato in vivo, demonstramos um efeito sinérgico exercido por uma combinação de PDE5i (vardenafil) e SERM (tamoxifeno). Tal sinergia sugere que quando as concentrações mais baixas desses medicamentos são administradas simultaneamente, o efeito líquido pode ser maior que a soma do efeito de cada medicamento. Tal abordagem sinérgica tem a vantagem adicional de utilizar os medicamentos em doses mais baixas e, portanto, reduzir o risco de eventos adversos.
Com base nesta evidência pré-clínica, começamos a tratar homens que se apresentaram em nossa clínica de andrologia com DP aguda (n = 102; dentro de 6 meses do início da doença), usando 5 mg de tadalafil uma vez ao dia e 20 mg de tamoxifeno duas vezes ao dia por 2 meses. Os medicamentos foram prescritos off-label de acordo com as diretrizes do Conselho Geral de Medicina do Reino Unido. O grupo controle (n = 45) consistiu de pacientes que receberam prescrição de vitamina E ou nenhum medicamento. Nossos resultados iniciais sugerem que significativamente mais pacientes que receberam a combinação tadalafil-tamoxifeno melhoraram na curvatura peniana (26,5%) do que aqueles no grupo controle (7,3%). Menos pacientes no grupo de combinação (12,7%) apresentaram piora da curvatura em comparação com os pacientes controle (26,8%). Atualmente, estamos no processo de expansão deste estudo preliminar, aumentando o número de pacientes e acompanhando-os por um período mais longo.
Outro estudo analisou retrospectivamente as alterações na curvatura peniana e na dor em homens (n = 47) com DP aguda durante o tratamento com tadalafil e tamoxifeno off-label em combinação com um dispositivo de ereção a vácuo (VED). Eles mostraram que após 12 semanas de tratamento, 57,4% dos pacientes não apresentaram melhora, 27,7% apresentaram melhora e 14,9% pioraram. O aumento gradual na melhoria ao longo de 12 semanas foi estatisticamente significativo.
Deve-se notar que os 2 estudos clínicos aqui mencionados foram apresentados em congressos de pesquisa em medicina sexual; não são publicações revisadas por pares. Ambos são estudos piloto com baixo número de pacientes. Além disso, eles têm outras limitações. Eles não são ensaios clínicos randomizados (ECR) e não são cegos ou controlados por placebo. No primeiro estudo, os pacientes que receberam a combinação tadalafil-tamoxifeno foram recrutados em um hospital diferente daqueles que receberam vitamina E ou nenhum medicamento. O segundo estudo não possui grupo controle e um dispositivo de ereção a vácuo foi adicionado à combinação. Apesar dessas advertências, acreditamos que há um sinal clínico para a maior taxa de melhora (25%-27%) com a combinação PDE5i-SERM em comparação com a resolução espontânea (3%-12%) relatada na literatura. Argumentamos que tal sinal justifica estudos clínicos maiores com controles apropriados.
Um ECR em grande escala seria caro e os incentivos financeiros para as empresas farmacêuticas financiarem ensaios tão caros seriam limitados por três razões. Primeiro, todos os PDE5is e SERMs não estão patenteados e as suas formulações genéricas estão agora no mercado. Isto torna improvável que um fabricante de medicamentos genéricos recupere os custos de ensaios clínicos tão dispendiosos e os custos de novo licenciamento. Em segundo lugar, o tamanho do mercado para a DP não é suficientemente grande para que um fabricante de medicamentos genéricos recupere os seus custos. Terceiro, sem alterar a formulação (o que representaria um custo adicional), a concorrência no mercado proveniente do uso off-label limitaria a exclusividade de mercado do medicamento reaproveitado.25 Além disso, o recrutamento de pacientes com DP aguda para um ensaio clínico em tão grande escala seria ser um desafio, pois a duração da doença no momento da apresentação pode variar de 4 a 6 meses a 10 a 17 meses.
Em conclusão, embora tenham surgido recentemente alguns sinais clínicos encorajadores que apoiam a noção de que uma combinação PDE5i-SERM pode ser eficaz para retardar ou interromper a progressão da DP aguda, ainda são necessárias evidências de alto nível na forma de ECRs.
Referência:
A combination of phosphodiesterase type 5 inhibitor and tamoxifen for acute Peyronie’s disease: the first clinical signals
Selim Cellek, MD, PhD, Matthew Megson, MBChB, Marcus M Ilg, PhD, David J Ralph, MS, FRCS (Urol)
The Journal of Sexual Medicine, Volume 20, Issue 8, August 2023, Pages 1057–1059, https://doi.org/10.1093/jsxmed/qdad083
Published:
04 July 2023